Les chéloïdes neuves traitées par la bléomycine en infiltration intra-lésionnelle chez des patients dans un pays ouest africain: Les résultats de l’expérience guinéenne (Conakry)
[New keloids treated with bleomycin intra-lesional infiltration in patients in a West African country: Resultats of the Guinean experience (Conakry)]
Moussa Savané 1,2, Boh Fanta Diané1,2, Mamadou Diouldé 1 Kante1,2, Mohamed Maciré Soumah1,2, Mariama Sadio Diallo1, Ahmed Sekou Keita1, Mamadou Thierno Tounkara1,2, Moussa Keita1,2, Mohamed Cisse1,2
1,2, Boh Fanta Diané1,2, Mamadou Diouldé 1 Kante1,2, Mohamed Maciré Soumah1,2, Mariama Sadio Diallo1, Ahmed Sekou Keita1, Mamadou Thierno Tounkara1,2, Moussa Keita1,2, Mohamed Cisse1,2
1Dermatology, Donka National Hospital, Conakry, Guinea, 2Faculty of Health Sciences and Techniques, University Gamal Abdel Nasser University of Conakry, Conakry, Guinea
Citation tools:
Copyright information
© Our Dermatology Online 2024. No commercial re-use. See rights and permissions. Published by Our Dermatology Online.
ABSTRACT
Introduction: Depending on their location and size, keloids often pose functional, aesthetic and even psychological problems. Black Africans and Asians are more prone to keloids, whereas they are rare in whites and albinos. Bleomycin has been reported as a means of treating keloids, but to our knowledge no study in black Africa has looked at this molecule in the treatment of keloids. The aim of this study is to evaluate the efficacy and safety of bleomycin in the treatment of new keloids by intracheloid infiltration in subjects with phenotype VI, who are the most predisposed to this condition.
Material and Methods: From 1 January to 31 December 2021, we identified 99 cases, 27 of whom met our inclusion criteria. They received intra-lesional bleomycin spaced 2 weeks apart or more for some with clinical parameters to evaluate the treatment. We judged the evolution: satisfactory, when pruritus and/or pain disappeared, the keloid mass subsided; more or less satisfactory, when pruritus and/or pain decreased, the keloid mass subsided; unsatisfactory, when pruritus and/or pain persisted, the keloid mass remained unchanged. Our data were processed and analysed using Epi Info 7.2.2.6.
Results: The mean age of the patients was 30.70 years, with extremes of 2 and 85 years. The sex ratio was 1.25. The major functional sign was isolated pruritus in 66.66%. The consistency of the lesions was hard in 11%. The median number of infiltrations was 3, with extremes of 1 and 5. The local effects observed were pain on infiltration in 92% and necrosis in 77.77% of cases. No systemic effects were noted. Treatment efficacy was satisfactory in 66.66% of cases.
Conclusions: Although bleomycin is less available in our countries and less accessible to patients, it could be proposed as a treatment for keloids, although a large study would be needed to evaluate it in large keloids.
Key words: New keloids; Bleomycin; Phenotype VI
RÉSUMÉ
Introduction: Les chéloïdes posent souvent, selon leur localisation et leur taille, des problèmes d’ordre fonctionnel, esthétique voire psychologique. Les noirs d’Afrique et les asiatiques sont plus exposés aux chéloïdes, alors qu’elles sont rares chez le blanc et l’albinos. La bléomycine est rapportée comme moyen de traitement de chéloïdes, mais à notre connaissance aucune étude en Afrique noire ne s’est intéressée à cette molécule dans le traitement des chéloïdes. Le but de cette étude est d’évaluer l’efficacité et la tolérance de la bléomycine dans le traitement des chéloïdes neuves par infiltration intra-chéloïdienne chez des sujets de phénotype VI qui sont les plus prédisposés à faire cette affection.
Matériel et Méthodes: Du 1er janvier au 31 décembre 2021, nous avons recensé 99 cas, dont 27 répondaient à nos critères d’inclusion. Ils ont reçu de la bléomycine en intra-lésionnelle espacée de 2 semaines voire plus pour certains avec des paramètres cliniques d‘évaluation du traitement. Nous avons jugé l’évolution: Satisfaisante, quand le prurit et/ou la douleur disparait, la masse chéloïdienne s’affaisse; plus ou moins satisfaisante, quand le prurit et/ou la douleur diminue, la masse chéloïdienne s’affaisse; non satisfaisante, quand le prurit et/ou la douleur persiste, la masse chéloïdienne reste inchangée. Nos données ont été traitées et analysées avec l’Epi Info 7.2.2.6.
Résultats: L’âge moyen des patients était de 30,70 ans avec des extrêmes de 2 et 85 ans. Le sex-ratio a été de 1,25. Le signe fonctionnel majeur était le prurit isolé chez 66,66 %. La consistance des lésions était dure dans 11%. Le nombre médian d’infiltration a été de 3 avec des extrêmes de 1 et 5. Les effets locaux observés ont été la douleur à l’infiltration dans 92% et la nécrose chez 77,77% des cas. Aucun effet systémique n’a été noté. L’efficacité du traitement a été satisfaisante dans 66,66%.
Conclusions: La bléomycine bien que moins disponible dans nos contrées et moins accessibles par les patients pourrait être proposé dans le traitement des chéloïdes, bien qu’une étude de grande taille serait nécessaire pour l’évaluer aussi dans des chéloïdes de grande taille.
Mots clés: Chéloïde neuve; Bléomycine; Phénotype VI
INTRODUCTION
Les chéloïdes posent souvent, selon leur localisation et leur taille, des problèmes d’ordre fonctionnel, esthétique voire psychologique [1,2]. Les noirs d’Afrique et les asiatiques sont plus exposés aux chéloïdes, alors qu’elles sont rares chez le blanc et l’albinos [3]. Au Congo Brazzaville l’incidence de la chéloïde est de 2,5 % [4], au Burkina Faso 0,4% [4]. A l’heure actuelle, il n’existe aucun consensus sur le traitement des chéloïdes [3,5]. Il est basé sur plusieurs moyens utilisés seul ou en association [6–10]. La bléomycine est rapportée comme moyen de traitement de chéloïdes [11,12], mais à notre connaissance aucune étude en Afrique noire ne s’est intéressée à cette molécule dans le traitement des chéloïdes. Elle reste coûteuse et moins accessible dans nos contrées. La bléomycine est un antibiotique antitumoral de nature glycopeptidique, isolée de streptomyces verticillus [13]. C’est un antimitotique utilisé en cancérologie [14]. Le but de cette étude est d’évaluer l’efficacité et la tolérance de la bléomycine dans la prise en charge des chéloïdes neuves par infiltration intra-chéloïdienne chez des sujets de phénotype VI qui sont les plus prédisposés à faire cette affection.
MATÉRIELS ET MÉTHODES
Nous avons mené une étude descriptive transversale d’une cohorte de patients, reçus dans le service de dermatologie de l’Hôpital National Donka, du 1er janvier au 31 décembre 2021. Le recrutement a consisté à identifier des patients atteints de chéloïde neuve (qui n’avaient pas encore reçu de traitement pour leur chéloïde). Tous ces patients atteints de chéloïde ont été inclus sans distinction de sexe, d’âge, ni de provenance et ayant accepté de bénéficier de l’infiltration intra lésionnelle de bléomycine après avoir obtenu leur consentement éclairé pour l’étude. Le diagnostic de la chéloïde a été clinique et aucune biopsie n’a été effectuée. Un bilan pré-thérapeutique et de suivi a été réalisé. Les patients atteints de chéloïdes de taille supérieure à 10 cm et parfois nécessitant une chirurgie n’ont pas été inclus. Les femmes enceintes ou allaitantes, les insuffisants rénaux et les perdus de vue n’ont pas également été inclus. Tous les patients inclus ont reçu de la bléomycine 15UI selon la technique suivante: La solution a été obtenue en diluant la Bléomycine 15UI poudre avec de l’eau distillée 10 ml et 2 ml de xylocaïne 2%. L’l’infiltration qui consistait à injecter dans la chéloïde la solution préparée. Les séances d’infiltration étaient pratiquées à des intervalles de 2 semaines ou plus pour certains patients qui ont présenté la nécrose de la chéloïde. Un nombre d’infiltration maximal de 10 a été fixé, qui correspond à la moitié de la dose cumulative qu’on ne doit pas dépasser au risque de fibrose pulmonaire en cas de son utilisation systémique. Avant chaque séance des photographies numériques étaient réalisées pour permettre d’apprécier l’évolution des chéloïdes. Les lésions sous traitement ont été appréciée sur:
- La persistance ou la disparition des signes suivants: prurit, douleurs.
- La persistance ou l’affaissement de la masse chéloïdienne (apprécié par la mensuration et les photographies numériques comparatives).
Nous avons jugé l’évolution:
Satisfaisante: quand le prurit et/ou la douleur disparait, la masse chéloïdienne s’affaisse.
Plus ou moins satisfaisante: quand le prurit et/ou la douleur diminue, la masse chéloïdienne s’affaisse. Non satisfaisante: quand le prurit et/ou la douleur persiste, la masse chéloïdienne reste inchangée. Nos données ont été traitées et analysées avec l’Epi Info 7.2.2.6.
RÉSULTATS
Quatre-vingt-dix-neuf patients ont été recensé sur 6558 consultants soit une fréquence de 1,5%. Sur ces 99 patients 27 répondaient à nos critères d’inclusion. Nous avons trouvé dans la tranche d’âge de 20 à 29 ans 9 patients, de 10 à 19 ans et de 30 à 39 ans, 6 patients chacune. Pour les patients de 0 à 9 ans 1 patient et supérieur à 60 ans 3 patients. L’âge moyen des patients était de 30,70 ans avec des extrêmes de 2 et 85 ans. Le sex-ratio était de 1,25. Les symptômes étaient le prurit isolé dans 66,66 %, douleurs isolées 22,22 %, prurit-douleurs 22,22 % et gène de la vie quotidienne 37,03% des cas. Les lésions étaient dure dans 11% des cas et ferme dans 89%. Le nombre médian d’infiltration a été de 3 avec des extrêmes de 1 et 5. Les effets locaux observés ont été la douleur à l’infiltration dans 92% des cas et la nécrose 77,77%. Les douleurs locales résiduelles et le durcissement de la chéloïde dans 7,40% chacun. Aucun effet systémique n’a été noté. L’efficacité du traitement a été satisfaisante dans 66,66%, plus ou moins efficace dans 18,51% et non satisfaisante 14,83 %.
DISCUSSION
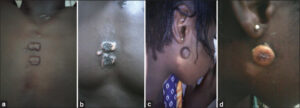
Les limites de cette étude ont été le facteur temps dans l’appréciation à long terme de l’efficacité du traitement. La fréquence hospitalière trouvée est inférieure à celle de Pitché P et al. au Togo (1,93 %) [6] et supérieure à celle de Adegbidi H et al. au Benin (0,7 %) [15] alors qu’en Europe elle varie de 6 à 16 % [16], ces différences s’expliqueraient par le fait que la chéloïde est sous-évaluée en Afrique de l’ouest pour des raisons mystico-religieuses [17]. Age moyen de nos patients est inférieur à celui trouvé par M. Mseddi et al 37,7 ans [14] et supérieur à celui trouvé par Assi K et al. 28 ans [1]. Il ressort de notre étude que la chéloïde n’est pas l’apanage des sujets jeunes qui ont une grande capacité à synthétiser du collagène mais peut se voir chez les personnes âgées. Nous avons trouvé une prédominance masculine. Ce qui ne contraste pas avec les données de la littérature comme souligne Assi k et al. qui ont noté qu’il n’y avait pas de prédominance de sexe [16], par contre A. Lahiri et al. ont trouvé une prédominance féminine dans 70 % des cas [18], K. Kibadi et al. 61 % et Niang S. et al. 42 femmes contre 21 hommes. Les chéloides étaient acquises dans 66,66% (Tableau 1), le tronc était le premier siège des chéloïdes dans notre série suivi des membres supérieurs et de la région cervico-céphalique (Tableau 2). Ces résultats sont proches à celles de M. Mseddi et al qui ont trouvé que les chéloïdes prédominaient au tronc 48 % des cas et aux membres supérieurs 34 % des cas [14], G. H. Yedomon et al. ont trouvé au tronc (34,53 %), au visage (10,65 %) et les bras (8,21 %) [1]. Ces localisations fréquentes s’expliqueraient par le fait que les chéloïdes surviennent dans les zones où la production du sébum est maximale et qui sont l’apanage de l’homme seul mammifère possédant des glandes sébacées [16]. La consistance des chéloïdes était ferme dans la majorité des cas. Ce résultat est opposé à ceux trouvés par Niang S. et al. (dure dans 50,8 % des cas et ferme dans 47,6 %) [18] et M. Mseddi et al. (dure dans 58 % des cas et ferme dans 42 % des cas) [14]. Le nombre médian d’infiltration par patient dans notre série a été inférieur à celui de J. Dutel-charneux et al. qui ont noté dans leur étude que le traitement a nécessité un nombre médian de 4 séances par patient (extrême de 2 et 6) [19]. Les effets locaux observés étaient dominés par les douleurs à infiltration suivies de la nécrose de la chéloïde (Figs. 1a – 1d), résultats proches de ceux trouvés par J. Dutel-charneux et al. qui ont noté que tous les patients rapportaient des douleurs importantes à l’infiltration et que 41 % des cas ont présenté la nécrose de la chéloïde. Aucun effet systémique n’a été observé comme J. Dutel-charneux et al. l’avait remarqué J Duteul-Charneux [19]. L’efficacité du traitement a été satisfaisante presque dans 66,66 % des cas, très proche à ce qui a été trouvé par Reddy R et al. où 65% ont eu une excellente réponse [11]; et A Espana et al. [20], ce qui vient démontrer la place de la bléomycine dans le traitement des chéloïdes.
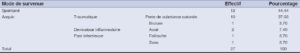 |
Tableau 1: Répartition des patients atteints de chéloïde selon le mode de survenue. |
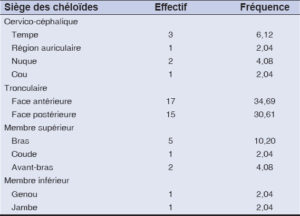 |
Tableau 2: Siège des Chéloïdes. |
Statement of Human and Animal Rights
All the procedures followed were in accordance with the ethical standards of the responsible committee on human experimentation (institutional and national) and with the 2008 revision of the Declaration of Helsinki of 1975.
Statement of Informed Consent
Informed consent for participation in this study was obtained from all patients.
REFERENCES
1. Yedomon GH, Adegbidi H, Atadokpede F, Akpadjan F, Mouto EJ, do Ango-Padonou F. Keloids on dark skin:a consecutive series of 456 cases. Med Sante Trop. 2012;22:287-291.
2. Carmassi M, Eraud J, Gonelli D, Magalon G, Andrac Meyer L. Cicatrices chéloïdes:étude d’une série de cas. Annales de Pathologie. 2015;35:148-53.
3. Allah KC, Yéo S, Kossoko H, Assi DjèBi DjèV, Richard Kadio M. Cicatrices chéloïdes sur peau noire :mythe ou réalité. Annales de Chirurgie Plastique Esthétique. 2013;58:115-22.
4. Boui M, Lemnaouer A. Dermatological experience at the Moroccan mobile field hospital in Brazzaville, Congo. Med Trop (Mars). 2009;69:13-7.
5. Jaloux C, Bertrand B, Degardin N, Casanova D, Kerfant N, Philandrianos C. Keloid scars (part II):Treatment and prevention. Ann Chir Plast Esthet. 2017;62:87-96.
6. PitchéP, KombatéK, Barruet K, Tchangaï-Walla K. Giant cheloid scars. Ann Dermatol Venereol. 2000;127:333.
7. Maalej M, Frikha H, Bouaouina N, Daoud J, Besbes M, Benna F, et al. Place de la curiethérapie dans le traitement des chéloïdes. Àpropos de 114 cas. Cancer/Radiothérapie. 2000;4:274-8.
8. Bimbi C, Brzezinski P. Combined treatment of keloids and scars with Nd:YAG 1064 nm laser and cryotherapy:Report of clinical cases. Our Dermatology Online. 2020;11:149-53.
9. Bukhari IA. Pulse dye laser therapy and superficial cryotherapy as a novel combination treatment for hypertrophic scars and keloids. Our Dermatol Online. 2022;13:28-31.
10. Uzair M, Butt G, Khurshid K, Suhail Pal S. Comparison of intralesional triamcinolone and intralesional verapamil in the treatment of keloids. Our Dermatol Online. 2015;6:280-4.
11. Reddy R, Harinatha S, Raghunath N. The role of Bleomycin in management of hypertrophic scars and keloids –A clinical trial. Our Dermatol Online. 2015;6:404-6.
12. Ledon JA, Savas J, Franca K, Chacon A, Nouri K. Intralesional Treatment for Keloids and Hypertrophic Scars:A Review. Dermatol Surg. 2013;39:1745-57.
13. Betarbet U, Blalock TW. Keloids:A review of etiology, prevention, and treatment. J Clin Aesthet Dermatol. 2020;13:33-43.
14. Mseddi M, Mesrati H, Ktaari S, Amouri M, Chaaben H, Boudaya S, et al. Treatment of keloid with phenol:a new therapy. Ann Dermatol Venereol. 2014;141:493-9.
15. Adegbidi H, Atadokpede F, do Ango-Padonou F, Yedomon H. Keloid acne of the neck:epidemiological studies over 10 years. Int J Dermatol. 2005;44:49-50.
16. Lahiri A, Tsiliboti D, Gaze NR. Experience with difficult keloids. Br J Plast Surg. 2001;54:633-5.
17. Pitche P. Quelle est la réalitédes chéloïdes “ spontanées “ ?Ann Dermatol Venereol. 2006;133:501.
18. Niang SO, Sankale A, Fall F, Diallo M, Dieng MT, Kane A. La place de la chirurgie dans la prise en charge des chéloïdes àDakar. Med Afr N. 2009;56:218-20.
19. Dutel-Charneux J, ReguiaïZ, Bernard P. Traitement des cicatrices chéloïdes par injections intra-lésionnelles de bléomycine :résultats àcourt et long terme. Ann Dermatol Venereol. 2012;139:277-8.
20. España A, Solano T, Quintanilla E. Bleomycin in the treatment of keloids and hypertrophic scars by multiple needle punctures. Dermatol Surg. 2001;27:23-7.
Notes
Request permissions
If you wish to reuse any or all of this article please use the e-mail (brzezoo77@yahoo.com) to contact with publisher.
| Related Articles | Search Authors in |
|
 http://orcid.org/0000-0003-3149-2987 http://orcid.org/0000-0003-3149-2987 http://orcid.org/0000-0003-1371-5198 http://orcid.org/0000-0003-1371-5198 http://orcid.org/0000-0002-1922-7075 http://orcid.org/0000-0002-1922-7075 http://orcid.org/0000-0003-2794-7870 http://orcid.org/0000-0003-2794-7870 |




Comments are closed.