Les toxidermies au cours de la grossesse: aspects clinique, étiologique et évolutif au CHU de Conakry (Guinée)
[The cutaneous drug reactions during pregnancy: clinical, etiological and evolutionary aspects at the University Hospital of Conakry (Guinea)]
Mohamed Maciré Soumah 1, Moussa Keita1, Thierno Mamadou Tounkara1, Boh Fanta Diane1, Demba Gninthé Soumah1, Fodé Bangaly Sako2, Fatimata Keita1, Mmah Aminata Bangoura3, Moussa Savane1, Mamadou Diouldé Kante1, Tely Sy4, Mohamed Cisse1
1, Moussa Keita1, Thierno Mamadou Tounkara1, Boh Fanta Diane1, Demba Gninthé Soumah1, Fodé Bangaly Sako2, Fatimata Keita1, Mmah Aminata Bangoura3, Moussa Savane1, Mamadou Diouldé Kante1, Tely Sy4, Mohamed Cisse1
1Department of Dermatology-STD, University Theaching Hospital of Donka, Gamal Abdel Nasser University of Conakry, Guinea, 2Department of Infectious and Tropical Deseases, University Theaching Hospital of Donka, Gamal Abdel Nasser University of Conakry, Guinea, 3Department of Pediatrics, University Theaching Hospital of Donka, Gamal Abdel Nasser University of Conakry, Guinea, 4Department of Maternity, University Theaching Hospital of Ignace Deen, Gamal Abdel Nasser University of Conakry, Guinea
How to cite this article: Soumah MM, Keita M, Tounkara TM, Diane BF, Soumah DG, Sako FB, Keita F, Bangoura MA, Savane M, Kante MD, Sy T, Cisse M. The cutaneous drug reactions during pregnancy: clinical, etiological and evolutionary aspects at the University Hospital of Conakry (Guinea). Our Dermatol Online. 2022;13(e):e60.
Submission: 15.09.2022; Acceptance: 05.11.2022
DOI: 10.7241/ourd.2022e.60
Citation tools:
Copyright information
© Our Dermatology Online 2022. No commercial re-use. See rights and permissions. Published by Our Dermatology Online.
ABSTRACT
Background: The cutaneous drug reaction is a real public health problem because of its very high mortality rate and its significant functional impact. Their occurrence during pregnancy is increasingly reported. They present an additional seriousness in this field which can put at risk the maternal-fetal prognosis. The aim of this study was to describe the clinical, etiological and evolutionary particularities of toxidermia during pregnancy.
Material and methods: This was a retrospective cross-sectional study from January 2000 to December 2021, covering cases of cutaneous drug reaction occurring during pregnancy and recorded in the Dermatology-STD department of the University Hospital of Conakry. The study consisted in identifying and documenting all these cases. The cases included were confirmed by a senior dermatologist; an obstetrical and neonatological consultation was obtained. We studied the sociodemographic, clinical, etiological and evolutionary data.
Results: We collected 19/204 (9.3%) cases of cutaneous drug reaction in pregnancy during the study period; the mean age was 23.15 years; 9/19 (47.3%) of the patients were primiparous. The type of cutaneous drug reaction was Stevens-Johnson syndrome (SJS)/Toxic Epidermal Necrolysis (TEN) in 13/19 (68.4%), maculo-papular exanthema (MPE) in 3/19 (15.8%), fixed bullous erythema pigmentosa in 2/19 (10.5%) and drug-induced urticaria in 1/19 (5.3%). HIV infection was found in 6/19 (31.6%) patients. The causal drug was found in 17/19 (89.5%) cases including antimalarials in 7/19 (36.8%), nevirapine and non-steroidal anti-inflammatory drugs in 4/19 (21.0%) cases each. We recorded 7/19 (36.8%) cases of spontaneous abortion; 3/19 (15.8%) cases of stillbirth and 9/19 (47.3%) cases of maternal-fetal death.
Conclusion: This study shows that the occurrence of cutaneous drug reactions during pregnancy is a challenge for the entire medical team, particularly at an early stage of gestation, especially in the case of severe forms that can affect the maternal and foetal prognosis.
Keywords: Cutaneous drug reactions, Pregnancy, SJS/NET, HIV, Conakry.
RÉSUMÉ
Introduction: Les toxidermies constituent un véritable problème de santé publique du fait de leur mortalité très élevée et de leur retentissement fonctionnel important. Leur survenue au cours de la grossesse est de plus en plus rapportée. Elles présentent une gravité supplémentaire sur ce terrain pouvant mettre en jeu le pronostic materno fœtal. Le but de cette étude était de décrire les particularités clinique, étiologique et évolutive des toxidermies au cours de la grossesse.
Matériel et méthodes: Il s’agissait d’une étude transversale rétrospective descriptive de Janvier 2000 à Décembre 2021, portant sur les cas de toxidermie survenue au cours de la grossesse et enregistrée au service de Dermatologie-MST du CHU de Conakry. L’étude a consisté à recenser et à documenter tous ces cas. Les cas inclus ont été confirmés par un dermatologue sénior; une consultation obstétricale et néonatologiste ont été obtenus. Nous avons étudié les données sociodémographique, clinique, étiologique et évolutive.
Résultats: Nous avons colligé 19/204 (9, 3 %) cas de toxidermie au cours de la grossesse durant la période d’étude; l’âge moyen était de 23, 15 ans; 9/19 (47, 3 %) des patientes étaient des primipares. Les toxidermies rencontrées étaient à type de syndrome de Stevens-Johnson (SSJ)/Nécrolyse épidermique toxique (NET) dans 13/19 (68, 4 %) cas, d’exanthème maculo-papuleux (EMP) dans 3/19 (15, 8 %) cas, d’érythème pigmenté fixe bulleux dans 2/19 (10, 5 %) cas et d’urticaire médicamenteuse dans 1/19 (5, 3 %). L’infection par le VIH a été retrouvée chez 6/19 (31, 6 %) patientes. Le médicament responsable a été retrouvé dans 17/19 (89, 5 %) cas dont les antipaludéens dans 7/19 (36, 8 %), la névirapine et les anti-inflammatoires non stéroïdiens dans 4/19 (21, 0 %) cas chacun. Nous avons enregistré 7/19 (36, 8 %) cas d’avortement spontané; 3/19 (15, 8 %) cas de mort-nés et 9/19 (47, 3 %) cas de décès materno-fœtal.
Conclusion: Il ressort de cette étude, que la survenue d’une toxidermie au cours de la grossesse est un défi pour l’ensemble de l’équipe médicale, en particulier à un stade précoce de la gestation surtout les formes graves qui peuvent mettre en jeu le pronostic materno-fœtal.
Mots clés: Toxidermies, Grossesse, SSJ/NET, VIH, Conakry
INTRODUCTION
Les toxidermies constituent les accidents médicamenteux les plus fréquemment rapportés dans les centres de pharmacovigilance dans le monde: environ 20 % des notifications d’accidents médicamenteux. Elles compliquent 2 à 3 % des traitements hospitaliers et motivent 1 % des consultations et 5 % des hospitalisations en dermatologie [1,2].
Néanmoins, plus de 90 % de ces toxidermies sont bénignes. Les formes sévères qui engagent le pronostic vital sont très rares (1 cas pour 10 000 à 1 000 000 patients traités) [3]; mais elles nécessitent une prise en charge rapide surtout sur des terrains particuliers comme la grossesse afin de minimiser des conséquences graves tant pour la gestante que pour son fœtus [4,5].
En effet, la survenue des toxidermies au cours de la grossesse est de plus en plus rapportée, leur gravité sur ce terrain fragile présente pour la gestante des troubles allant de l’inconfort à un risque d’engagement du pronostic vital [4]. Pour le fœtus les conséquences des toxidermies sont tout aussi graves (retard de croissance, prématurité, faible poids à la naissance, avortements, mortalités post natal).
Les données concernant cette affection sur ce terrain sont parcellaires et concernent pour la plupart les gestantes infectées par le virus de l’immunodéficience humaine (VIH) [4–7].
Ces toxidermies graves sur grossesse doivent attirer l’attention de tout praticien et être notifiées aux instances de pharmacovigilance pour permettre une évaluation correcte du rapport bénéfice/risque des médicaments [3].
Le but de cette étude était de décrire les particularités clinique, étiologique et évolutive des toxidermies au cours de la grossesse.
MATÉRIEL ET METHODS
Il s’agissait d’une étude transversale rétrospective descriptive de Janvier 2000 à Décembre 2021, portant sur les cas de toxidermie survenue au cours de la grossesse et enregistrée au service de Dermatologie-MST du CHU de Conakry. Ce service est l’unique du genre dans notre pays. Il prend en charge toutes les maladies de peau y compris les réactions cutanées aux médicaments, représentant ainsi un maillon important de la pharmacovigilance en Guinée. L’étude a consisté à recenser et à documenter tous ces cas.
Nous avons inclus dans cette étude, toutes les gestantes chez lesquelles le diagnostic de toxidermie a été retenu, confirmé par un dermatologue sénior, quelque soit l’âge gestationnel et le type de toxidermie. Tous les cas inclus ont eu un avis gynéco-obstétrical et de la néonatologie pour les nouveaux nés.
Les critères diagnostiques de toxidermie, internationalement reconnus ont été également utilisés pour certaines formes [8,9].
Nous avons aussi inclus dans cette étude, les deux cas de syndrome de Lyell déjà publiés par notre service [4].
Les critères d’imputabilité utilisés pour établir la responsabilité des médicaments incriminés étaient celle de la pharmacovigilance française de Begaud et al [10]. Ces critères ont été systématiquement recherchés selon les données de l’EuroSCAR-Study [11].
Nous avons étudié les données:
- Sociodémographique: âge, statut matrimonial, résidence, niveau d’instruction;
- Clinique: antécédent d’allergie médicamenteuse, parité, âge gestationnel, comorbité associée (VIH, diabète), délai de survenu; type de toxidermie;
- Etiologique: médicaments incriminés;
- Evolutive: durée d’hospitalisation, suites évolutives, évolution materno-fœtale (issue de la grossesse, survie materno-fœtale).
Les données ont été recueillies sur des fiches d’enquête, saisies dans les logiciels Word puis analysées dans Excel.
Cette étude a été approuvée par le comité éthique de la faculté de Médecine de l’université Gamal Abdel Nasser de Conakry.
RÉSULTATS
Sur 204 cas de toxidermie enregistrée durant la période d’étude au service de Dermatologie-MST, nous avons dénombré 19 (9,3 %) cas survenus au cours de la grossesse; il s’agissait de jeunes femmes avec une moyenne d’âge de 23,15 ans et des extrêmes de 16 ans et de 34 ans; la tranche d’âge de 16 à 25 ans était la plus touchée soit 13/19 (68,4 %) cas, elles étaient mariées dans 16/19 (84,2 %) cas, analphabètes dans 11/19 (57,9 %) cas et vivaient en zone urbaine dans 15/19 (78,9 %) cas. Les caractéristiques sociodémographiques des patientes sont récapitulées dans le tableau I.
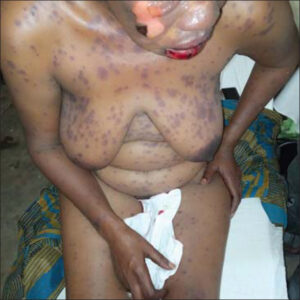
Sur le plan clinique, 9/19 (47, 3 %) des patientes étaient des primipares avec un âge gestationnel moyen de 16 semaines d’aménorrhée et des extrêmes de 4 à 28 semaines d’aménorrhée; la toxidermie était survenue au cours du premier trimestre de la grossesse dans 11/19 (57, 8 %) et du deuxième trimestre chez 5/19 (26, 3 %) patientes; la majorité des toxidermies est survenue entre 7 et 21 jours après le début de la prise du médicament suspect; l’infection par le VIH a été retrouvée chez 6/19 (31, 6 %) patientes. Les toxidermies rencontrées étaient à type de syndrome de Stevens-Johnson (SSJ)/Nécrolyse épidermique toxique (NET) dans 13/19 (68, 4 %) cas (Figs. 1a–1d and 2), d’exanthème maculo-papuleux (EMP) dans 3/19 (15, 8 %) cas, d’érythème pigmenté fixe bulleux dans 2/19 (10, 5 %) cas et d’urticaire médicamenteuse dans 1/19 (5, 3 %) cas. Le tableau II récapitule les caractéristiques cliniques des patientes.
 |
Tableau II: Caractéristiques cliniques des patientes. |
Sur le plan étiologique, le médicament responsable a été retrouvé dans 17/19 (89, 5 %) cas. Il s’agissait des antipaludéens dans 7/19 (36, 8 %), administrés pour la chimio prophylaxie contre le paludisme au cours de la grossesse, dont la Quinine dans 2/19 (10, 5 %) cas et la Sulfadoxine-Pyrimethanine (SP) dans 5/19 (26, 3 %) cas, de la Névirapine dans 4/19 (21, 0 %) cas administrée en association avec d’autres antirétroviraux pour la prévention de la transmission mère-enfant (PTME) du VIH, des anti-inflammatoires non stéroïdiens dans 4/19 (21, 0 %) cas dont l’Ibuprofène et le Diclofenac dans 2/19 (10, 5 %) cas chacun, et du Sulfametoxazole-Trimetoprime (Cotrimoxazole) dans 2/19 (10, 5 %) cas; dans 2/19 (10, 5 %) cas la nature du médicament responsable n’a pas pu être identifiée.
Sur le plan évolutif, la durée moyenne de séjour était de 16,5 jours avec des extrêmes de 1 à 32 jours; nous avons enregistré 7/19 (36, 8 %) cas d’avortement spontané; 3/19 (15,8 %) cas de mort-nés, 2/19 (10,5 %) cas de décès post-natal et 9/19 (47,3 %) cas de décès materno-fœtal.
DISCUSSION
De janvier 2000 à Décembre 2021, nous avons réalisé une étude transversale de type descriptif à recrutement rétrospectif sur dossiers de patient hospitalisés, afin de documenter les cas de toxidermies au cours de la grossesse dans notre service.
Le caractère rétrospectif de cette étude ne nous a pas permis de cerner tous les aspects de ce problème. Néanmoins, les résultats auxquels nous sommes parvenus permettent de décrire les caractéristiques sociodémographiques, cliniques, étiologiques et évolutives des toxidermies au cours de la grossesse dans le service de Dermatologie – MST du CHU Donka.
Avec 19 cas colligés en 21 ans, notre étude confirme la rareté des toxidermies au cours de la grossesse surtout les formes graves survenant sur des terrains particuliers comme le VIH. Cependant, ce chiffre ne reflète pas exactement la réalité.
En effet le caractère rétrospectif de notre étude, le système de référence des patients et le recours à la médecine traditionnelle (couramment utilisé en première intension), ne permettent pas de voir tous les cas de toxidermie, bien que notre service soit l’unique du pays pour la prise en charge des maladies de la peau.
Les cas rapportés concernent le plus souvent les formes graves à type de SSJ/NET, où la plus grande série provient de l’Afrique du Sud avec 22 cas rapportés en 4 ans pour un seul centre [7].
Dans notre série comme dans d’autres, la plupart des parturientes ont moins de 40 ans. Un âge considéré comme faible facteur de risque de mortalité selon le SCORTEN [12].
Contrairement à notre série où nous n’avons pas trouvé de prédominance chez les patientes infectées par le VIH, il est bien établi que l’incidence des toxidermies notamment des formes graves comme le SSJ/NET, augmente avec l’infection par le VIH.
Sur le plan étiologique, les médicaments classiques sont souvent incriminés. L’utilisation de la nevirapine dans la PTME du VIH pendant la période d’étude a été la principale raison de cette incidence plus élevée. La fréquence des toxidermies dues à la névirapine varie entre 10 à 35 % selon les études [13–20]. Dans une méta-analyse des différentes cohortes sous névirapine, la fréquence des toxidermies, quelle que soit la gravité, était estimée à 35 % chez 380 malades traités par névirapine contre 19 % dans le groupe contrôle [15]. Dans la même population, les toxidermies étaient sévères dans 6,6 % dans le groupe névirapine contre 1,9 % dans le groupe contrôle. La fréquence des toxidermies graves due à la névirapine varie donc selon les auteurs. En effet, si dans la majorité des cas les toxidermies induites par la névirapine sont bénignes et restent largement dominées par les exanthèmes maculopapuleux, la fréquence des toxidermies sévères n’est pas négligeable [21–23]. Le risque de SSJ/NET chez les malades traités par névirapine est de 0,3 % [21].
Le degré du déficit immunitaire associé à la prise de névirapine jouerait un rôle dans la survenue du syndrome de Lyell chez les femmes enceintes. En effet selon Boehringer-Ingelhein, le fabricant de la névirapine, il existerait une probabilité accrue de toxicité tant hépatique que cutanée chez les femmes séropositives en général, prenant ce médicament en ayant des taux de CD4 supérieurs à 250/mm3.
Le retrait de la NVP dans des protocoles de PTME récemment introduits en Afrique pourrait contribuer à réduire cette incidence. Le problème reste avec les anti-paludéens qui continuent à être utilisés pour la prophylaxie et le traitement du paludisme. En effet, Le paludisme constitue un problème majeur de santé publique en Afrique subsaharienne [24]. Il présente des risques importants pour la mère, le fœtus et le nouveau-né [25]. C’est pourquoi sa prévention au cours de la grossesse demeure une préoccupation majeure. Cela s’est traduit par l’introduction du traitement préventif intermittent (TPI) avec la SP, pour la prévention du paludisme chez les femmes enceintes. Bien que ce TPI-SP soit bien toléré, il présente tout de même quelques risques, comme rapporté par Yavo JC et al [26], où 6,3 % des prescripteurs ont évoqué le risque de survenue de malformations fœtales et les risques allergiques (toxidermies). Ce risque de toxidermies à la SP, confirmé par notre étude, est également rapporté par d’autres auteurs, bien que cela soit survenu en dehors de la grossesse [27–29]. C’est pourquoi, une attention toute particulière, doit être portée à cette prophylaxie en recherchant systématiquement, une notion d’allergie aux sulfamides chez la femme enceinte, avant toute prescription des molécules recommandées.
Sur le plan évolutif, la survenue d’une toxidermie, surtout des formes graves, peut mettre en jeu le pronostic materno-fœtal, comme l’illustrent nos résultats. C’est pourquoi leur survenue chez la femme enceinte, est un défi pour toute l’équipe médicale, surtout à un stade précoce de la gestation. Le pronostique fœtal est marqué par des avortements, des naissances prématurées et les faibles poids de naissances, comme observées dans notre série. Ces naissances prématurées et l’hypotrophie fœtale sont plus fréquentes dans les cohortes de femmes infectées par le VIH que dans la population générale [30]. Aussi, plusieurs autres cohortes ont montré un taux accru d’accouchement prématuré associé à l’utilisation d’une multi thérapie antirétrovirale [31–33]. Cependant cette constatation reste sans explication physiopathologique, et nous ne pouvons pas dire s’il existe un lien de causalité entre la thérapie antirétrovirale et l’accouchement prématuré [6]. La naissance prématurée dans le cadre de la NET par exemple, pourrait être due à un stress fœtal dû à la maladie de la mère [34]. Le taux élevé de décès materno-fœtal au cours des formes graves, observé dans notre série n’est pas confirmé dans la littérature, qui suggère d’ailleurs un taux élevé de survie de la mère et du nouveau-né en cas de NET pendant la grossesse, comme rapporté par Knight L et al [7], ceci pourrait être le résultat d’un biais de publication [6]; car il est bien connu que la mortalité reste élevée au cours des formes graves de toxidermie.
RÉFÉRENCES
1. Thielen Klee AM, Toutous Trellu LM, Desmeules JA. Les toxidermies médicamenteuses. Rev Méd Suisse. 2008;4:1671-5.
2. Valeyrie-Allanore L, Sassolas B, Roujeau JC. Drug-induced skin, nail and hair disorders. Drug Saf. 2007;30:1011-30.
3. Lebrun-Vignes B, Valeyrie-Allanore L. Toxidermies. Rev Méd Inter. 2015;36:256-70.
4. CisséM, Soumah MM, Tounkara TM, DianéBF, Sako FB, BaldéH, et al. Lyell syndrome with fatal outcome in two pregnant women receiving antirétroviral therapy in Guinea Conakry. J Cosm Dermatol Scien Applicat:JCDSA. 2013;3:135-8.
5. Shilad A, Predanic M, Perni SC, Houlihan C, Principe D. Human immunodeficiency virus, pregnancy, and Stevens-Johnson syndrome. Obst Gynecol. 2005;105:1254-6.
6. Struck MF, Illert T, Liss Y, Bosbach ID, Reichelt B, Steen M. Toxic epidermal necrolysis in pregnancy:case report and review of the literature. J Burn Care Res. 2010;31:816-21.
7. Knight L, Todd G, Muloiwa R, Matjila M, Lehloenya RJ. Stevens Johnson syndrome and toxic epidermal necrolysis:maternal and foetal outcomes in twenty-two consecutive pregnant HIV infected women. PloS One. 2015;10:e0135501.
8. Bastuji-Garin S, Rzany B, Stern RS, Shear NH, Naldi L, Roujeau JC. Clinical classification of cases of toxic epidermal necrolysis, Stevens-Johnson syndrome and erythema multiforme. Arch Dermatol. 1993;129:92-6.
9. Auquier-Dunant A, Mockenhaupt M, Naldi L, Correia O, Schro- der W, Roujeau JC, et al. Severe cutaneous adverse reactions. Correlations between clinical patterns and causes of erythema multiforme majus, Stevens-Johnson syndrome, and toxic epidermal necrolysis:results of an international prospective study. Arch Dermatol. 2002;138:1019-24.
10. Begaud B, Evreux JC, Jouglard J, Lagier G. Imputabilitédes effets inattendus ou toxiques des médicaments. Actualisation de la méthode utilisée en France. Therapie. 1985;40:111-8.
11. Mockenhaupt M, Viboud C, Dunant A, Naldi L, Halevy S, Bouwes Bavinck JN et al. Stevens-Johnson syndrome and toxic epidermal necrolysis:assessment of medication risks with emphasis on recently marketed drugs. The EuroSCAR-study. J Invest Dermatol. 2008;128:35-44.
12. Bastuji-Garin S, Fouchard N, Bertocchi M, Roujeau JC, Revuz J, Wolkenstein P. SCORTEN:a severity-of-illness score for toxic epidermal necrolysis. J Invest Dermatol. 2000;115:149-53.
13. Milpied-Homsi B, Relliquet V, Huart A, Raffi F. Toxicitécutanée de la névirapine utilisée en première intention dans le traitement de 100 patients. Ann Dermatol Venereol. 1999;126:2S21.
14. Barner A, Myers M. Nevirapine and rashes. Lancet. 1998;351:1133.
15. Pollard RB, Robinson P, Dransfield K. Safety profile of nevirapine a nonnucleosid reverse transcriptase inhibitor for the treatment of HIV. Clin Ther. 1998;20:1071-92.
16. Knobel H, Miro JM, Mahillo B, Domingo P, Rivero A, Ribera E, et al. Failure of cetirizine to prevent nevirapine-associated rash:A double-blind placebo-controlled trial for the GESIDA 26/01 Study. J Acquir Immune Defic Syndr. 2004;37:1276-81.
17. Carr A, Vella S, de Jong MD, Sorice F, Imrie A, Boucher CA et al. Dutch-Italian-Australian Nevirapine Study Group. A controlled trial of nevirapine plus zidovudine versus zidovudine alone in p24 antigenaemic HIV-infected patients. AIDS. 1996;10:635-642.
18. Montaner JSG, Reiss P, Cooper D, Vella S, Harris M, Conway B et al. A Randomized, Double-blind Trial Comparing Combinations of Nevirapine, Didanosine, and Zidovudine for HIV-Infected Patients:The INCAS Trial. JAMA. 1998;279:930–7.
19. Bonnet F, Lawson-Ayayi R, Thiebaut R, Ramanampamonjy R, Lacoste D, Bernard N, et al. A cohort of nevirapine tolerance in clinical practice:French Aquitaine cohort 1997-1999. Clin Infect Dis. 2002;35:1231-7.
20. Caumes E, Bossi P, Katlama C, Bricaire F. Toxidermies dues aux antirétroviraux chez les patients infectés par VIH. Presse Med. 2003;32:1325-33.
21. Fagot JP, Mockenhaupt M, Bouwes-Bavinck JN, Naldi L, Viboud C,?Roujeau JC, et al. Nevirapine and the risk of Stevens-Johnson syndrome or toxic epidermal necrolysis. AIDS. 2001;15:1843-8.
22. Rotunda A, Hirsch RJ, Scheinfeld N, Weinberg JM. Severe cutaneous reactions associated with the use of human immunodeficiency virus medications. Acta Derm Venereol. 2003;83:1-9.
23. Bourezane Y, Salard D, Hoen B, Vandel S, Drobacheff C, Laurent R. DRESS (Drug Rash with Eosinophilia and Systemic Symptoms) Syndrome Associated with Nevirapine Therapy. Clin Infect Dis. 1998;27:1321-2.
24. Organisation mondiale de la santé. Paludisme:aide-mémoire No 94. Genève;2018.
25. Desai M, ter Kuile FO, Nosten F, McGready R, Asamoa K, Brabin B, et al. Epidemiology and burden of malaria in pregnancy. Lancet Infect Dis. 2007;7:93-104.
26. Yavo JC, Amari AS, Assi SB, Assemian A, KouaméR, Balayssac E, KamagatéM. Évaluation de la connaissance du traitement préventif intermittent au cours de la grossesse (TPIg) par la sulfadoxine-pyriméthamine en Côte d’Ivoire. Therapies. 2019;74:487-94.
27. Miller KD, Lobel HO, Satriale RF, Kuritsky JN, Stern R, Campbell CC. Severe cutaneous reactions among American travelers using pyrimethamine-sulfadoxine (FANSIDAR) for malaria prophylaxis. Am J Trop Med Hyg. 1986;35:451-8.
28. Kourouma S, Sangare A, Kologa M, Kouassi I, Ecra E, Gbery I, et al. Syndromes de Stevens-Johnson et de Lyell:Etude de185 cas au CHU de Treichville (Abidjan, Côte d’Ivoire). Méd SantéTrop. 2014;24:94-8.
29. Owono Etoundi P, Danwang C, Bengono Bengono R, AfanéEla A, Ze MinkandéJ. La nécrolyse épidermique toxique en milieu hospitalier camerounais. Méd Afriq Noire. 2016;63:583.
30. Brocklehurst P, French R. The association between maternal HIV infection and perinatal outcome:a systematic review of the literature and meta-analysis. Br J Obstet Gynaecol. 1998;105:836-48.
31. The European Collaborative Study and the Swiss Mother Child HIV Cohort Study. Combination antiretroviral therapy and duration of pregnancy. AIDS. 2000;14:2913-20.
32. Szyld EG, Warley EM, Freimanis L, Gonin R, Cahn PE, Calvet GA, Duarte G, Melo VH, Read JS;NISDI Perinatal Study Group. Maternal antiretroviral drugs during pregnancy and infant low birth weight and preterm birth. AIDS. 2006;20:2345-53.
33. Cotter AM, Garcia AG, Duthely ML, Luke B, O’Sullivan MJ. Is antiretroviral therapy during pregnancy associated with an increased risk of preterm delivery, low birth weight, or stillbirth?J Infect Dis. 2006;193:1195-201.
34. Claessens N, Delbeke L, Lambert J, Matthieu L, Lafaire C, Van Marck E. Toxic epidermal necrolysis associated with treatment for preterm labor. Dermatology. 1998;196:461-2.
Notes
Request permissions
If you wish to reuse any or all of this article please use the e-mail (brzezoo77@yahoo.com) to contact with publisher.
| Related Articles | Search Authors in |
|
 http://orcid.org/0000-0003-2794-7870 http://orcid.org/0000-0003-2794-7870 |




Comments are closed.