Etude épidémiologique, clinique, étiologique et thérapeutique des toxidermies médicamenteuses chez les patients infectés par le VIH dans deux Unités de Soins de Bamako, Mali
[Epidemiological, Clinical, Etiological and Therapeutic Study of Drug eruption in HIV-infected patients in the two Accompaniment Care Unit and Advice of Bamako, Mali]
Yamoussa Karabinta 1,2, Dienebou Niangaly1, Chata Traore1, Issa Konate3, Tenin Karambe4, Koureissi Tall1, Binta Guindo1, Mamadou Gassama1,2, Mamoudou Diakite1, Adama Anguissa Dicko1,2, Lydie Joelle Seudjip Nono5, Ousmane Faye1,2
1,2, Dienebou Niangaly1, Chata Traore1, Issa Konate3, Tenin Karambe4, Koureissi Tall1, Binta Guindo1, Mamadou Gassama1,2, Mamoudou Diakite1, Adama Anguissa Dicko1,2, Lydie Joelle Seudjip Nono5, Ousmane Faye1,2
1Department of Dermatology, Centre Hospitalier Universitaire de Dermatologie, Bamako, Mali, 2Faculty of Medicine and Odontostomatology University of Sciences, Techniques and Technologies of Bamako, Bamako, Mali., 3Department of Infectious Diseases, Centre Hospitalier Universitaire du Point G., Bamako, Mali, 4Department of Dermatology, Centre Hospitalier Universitaire Gabriel Toure, Bamako, Mali, 5Department of Dermatology, University Clinics of Kinshasa, Democratic Republic of Congo
Corresponding author: Yamoussa Karabinta, MD
How to cite this article: Karabinta Y, Niangaly D, Traore C, Konate I, Karambe T, Tall K, Guindo B, Gassama M, Diakite M, Dicko AA, Seudjip Nono LJ, Faye O. Etude épidémiologique, clinique, étiologique et thérapeutique des toxidermies médicamenteuses chez les patients infectés par le VIH dans deux Unités de Soins de Bamako, Mali [Epidemiological, Clinical, Etiological and Therapeutic Study of Drug eruption in HIV-infected patients in the two Accompaniment Care Unit and Advice of Bamako, Mali]. Our Dermatol Online. 2022;13(Supp. 1):1-6.
Submission: 15.12.2021; Acceptance: 01.02.2022
DOI:10.7241/ourd.2022S1.1
Citation tools:
Copyright information
© Our Dermatology Online 2022. No commercial re-use. See rights and permissions. Published by Our Dermatology Online.
ABSTRACT
Background: The increase in prescriptions of antiretrovirals (ARVs) implies the increasing occurrence of side effects, including skin manifestations. The objective of this work was to identify the epidemiological and therapeutic aspects of drug eruptions during ARV treatment in the support and counseling units (SCU) of commune IV of the district of Bamako.
Material and methods: In a documentary study, the data of patients living with HIV (PLHIV) followed in the SCUs between January 2008 and December 2010, i.e. 3 years, in strict respect of their confidentiality were collected. Parameters of interest included epidemiological, clinical and therapeutic characteristics.
Results: The frequency of drug eruptions was 2.85% of cases, ie 50 patients out of 1748 PLWHA. Women accounted for 76% of cases with a sex ratio of 0.32. The mean age was 30.8 ± 11.46 years with extremes ranging from 5 to 60 years. PLHIV were in WHO clinical stage III, or 48% of cases. The mean time to onset of drug eruption was 23.5 ± 17.7 days. Common clinical manifestations were pruritus (24%), rash (22%) and Lyell’s syndrome (12%). 96% of patients (48 cases) were on ARVs, of which 78% were on nevirapine and 14% on efavirenz. The treatment was symptomatic.
Conclusion: Antiretrovirals are sources of drug eruption despite their benefits in the treatment of HIV/AIDS. Rigorous monitoring is essential to prevent these harmful effects.
Key words: Drug eruption, Person living with HIV, Epidemio-clinical, Therapeutic, Bamako
RÉSUMÉ
Contexte: L’augmentation des prescriptions d’antirétroviraux (ARV) implique la survenue croissante des effets secondaires parmi lesquels les manifestations cutanées. L’objectif de ce travail était de relever les aspects épidémio-cliniques et thérapeutiques des toxidermies au cours du traitement ARV dans les unités de soins accompagnement et de conseils (USAC) de la commune IV du district de Bamako.
Matériel et méthodes: Dans une étude documentaire, les données des patients vivant avec le VIH (PVVIH) suivis dans les USAC entre janvier 2018 et décembre 2019, soit 24 mois, dans le respect strict de leur confidentialité étaient colligées. Les paramètres d’intérêts comprenaient les caractéristiques épidémiologiques, cliniques et thérapeutiques.
Résultats: La fréquence des toxidermies était de 2,85% des cas, soit 50 patients sur 1748 PVVIH. Les femmes représentaient 76% des cas avec un sex ratio de 0,32. L’âge moyen était de 30,8 ± 11,46 ans avec des extrêmes allant de 5 à 60 ans. Les PVVIH étaient au stade clinique III de l’OMS, soit 48% des cas. Le délai moyen de survenu de toxidermie était 23,5 ± 17,7jours. Les manifestations cliniques étaient fréquentes étaient le prurit (24%), l’exanthême (22%) et le syndrome de Lyell (12%). 96% des patients (48 cas) étaient sous ARV dont 78% sous névirapine et 14% sous efavirenz. Le traitement était symptomatique.
Conclusion: les antirétroviraux sont pourvoyeurs de toxidermies malgré leurs bénéfices dans le traitement du VIH/SIDA. Une surveillance rigoureuse s’avère indispensable pour prévenir ces effets néfastes.
Mots clés: Toxidermie, Personne vivant avec le VIH, Epidémio-clinique, Thérapeutique, Bamako
INTRODUCTION
Le traitement antirétroviral (ARV) a suscité beaucoup d’espoir en améliorant considérablement la survie des patients séropositifs. Il regroupe de nos jours plusieurs molécules [1] classées en inhibiteurs nucléotidiques et non nucléotidiques de la transcriptase inverse (INTI, INNTI), des protéases (IP) et de fusion et d’intégrase. Avec l’augmentation de la prescription d’ARV, on assiste à la survenue croissante des effets secondaires à l’instar des toxidermies. En effet, ces accidents cutanés sont évalués à 20% en Europe et répartis de la manière suivante: 1% comme symptôme dominant, 2 à 3% au cours des traitements hospitaliers et 5% des motifs d’hospitalisations en dermatologie [2]. Au Maroc, sur une période de dix ans, 35,14% des notifications du Centre Marocain de Pharmacovigilance sont représentées par les toxidermies dont 42,91% d’exanthèmes induits pour la plupart par les blactamines et sulfamides. Dans 68,5% des cas, ces accidents étaient graves [3]. En 2002 dans une étude menée à Cotonou, l’incidence de la nécrolyse épidermique toxique aiguë était de 3 cas/an [4]. Les études maliennes rapportent que l’érythème pigmenté fixe (EPF) était la toxidermie la plus fréquente, causée principalement par les sulfamidés [5]. Pour Caumes E en 2003 [6], les lésions cutanées représentaient respectivement 13,6% des effets secondaires observés au cours du traitement antirétroviral. Par ailleurs chez les personnes vivant avec le VIH (PVVIH), il a été estimé que le risque de toxidermie était multiplié par 4 à 30 selon les médicaments utilisés pour la prise en charge de cette infection [2].
L’objectif de cette étude était de relever les aspects épidémiologiques, cliniques et thérapeutiques des toxidermies médicamenteuses chez les PVVIH suivies dans la commune IV du district de Bamako et d’identifier les molécules responsables
MATÉRIEL ET MÉTHODES
Nature, durée et lieu de l’étude: Nous avons colligé les dossiers des patients suivis dans les USAC du CHU de dermatologie de Bamako et du centre de santé de référence de la commune IV du district de Bamako durant la période allant du 1er janvier 2018 au 30 décembre 2019, soit 24 mois. Etaient éligibles, toutes les PVVIH présentant une toxidermie médicamenteuse. Les dossiers ne comportant pas toutes les variables d’intérêt étaient exclus.
Paramètres d’intérêt
Les données répertoriées étaient épidémiologiques (âge, sexe, lieu de résidence, situation matrimoniale) cliniques (circonstances de découverte de l’infection à VIH, stade clinique de l’infection à VIH selon l’OMS, délai d’apparition de la toxidermie, aspect clinique de la toxidermie, médicaments consommés avant l’éruption cutanée), paracliniques (sérologie VIH et typage, taux de CD4) et thérapeutiques (médicaments incriminés).
Définitions opérationnelles: La toxidermie est une réaction cutanée et/ou muqueuse consécutive à une prise médicamenteuse (ARV et/ou médicaments contre l’infection opportuniste). Il s’agit de lésion à type de prurit, urticaire, exanthème, érythème polymorphe, érythème pigmenté fixe, érythrodermie, éruption lichénoïde, syndrome de Lyell, troubles pigmentaires, purpura et autre type de lésion cutanée.
Les données ont été recueillies sur un questionnaire pré-établi et pré-testé. Leurs traitement et analyse statistiques ont été réalisés à l’aide du logiciel EPI INFO 6.04 version française et les Saisies avec les logiciels Microsoft Word.
La confidentialité des données a été préservée tout le long des investigations.
RÉSULTATS
1- Données épidémiologiques
Au cours de notre étude, 1750 dossiers des PVVIH étaient examinés parmi lesquels 1474 étaient sous ARV. Les manifestations toxidermiques étaient retrouvées chez 2,85% des cas, soit 50 patients dont 48 sous ARV et 2 sans ARV. La tranche d’âge de 31 – 40 ans et de 41 – 50 ans étaient prédominantes respectivement dans 34 et 36% des cas. La moyenne d’âge était de 30,8 ± 11,46 ans avec des extrêmes allant de 4 à 60 ans.
2- Données cliniques
Les patients résidaient à Bamako dans 84% des cas (44 cas).
L’infection opportuniste était la circonstance de découverte de l’infection à VIH dans 66 % des cas. Le VIH-1 représentait 96% des cas.
La plus part des patients étaient au stade III du VIH dans 48% des cas.
Ces toxidermies avaient un délai d’apparition comprise entre 16-30 jours dans 38% (19 cas), inférieur à 15 jours dans 34% des cas (17 cas) et 31-40 jours dans 12% (6 cas). La réaction cutanée aux médicaments la plus fréquente était le prurit isolé dans 24% des cas.
Le temps écoulé entre le début du traitement et la survenue de la toxidermie variait en majorité entre 5 et 30 jours soit 72% avec une moyenne de 23,5 jours ± 17,7 jours avec des extrêmes allant de 5 à 90 jours.
Selon le tableau 1, la nevirapine ressort comme la principale molécule incriminée dans la survenue des toxidermies dans 48% des cas.
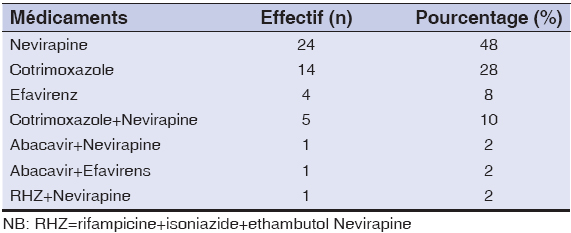 |
Tableau 1: Récapitulatif des médicaments ayant été incriminés dans la survenue des toxidermies. |
Le tableau 2 montre que la nevirapine est la plus impliquée dans la survenue des toxidermie (24 cas soit 48%), suivie du cotrimoxazole (14 cas soit 28%) dont pour lequel le délai de survenue de la toxidermie est inférieure ou égale à 15 jours.
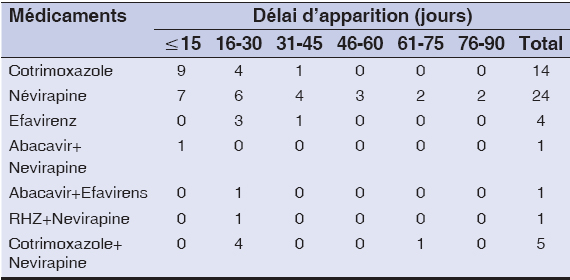 |
Tableau 2: Répartition des molécules incriminées en fonction du délai d’apparition des lésions cutanées. |
3- Données biologiques
Selon le tableau 3, la majeure partie des PVVIH (44% des 22 cas) avaient un taux de CD4 ≤ 200 avec une moyenne de 228,10 cellules/mm3
 |
Tableau 3: Répartition de l’effectif en fonction du taux de CD4. |
4- Données thérapeutiques
Sur le plan thérapeutique, les PVVIH sous D4T+FTC+NVP étaient les plus nombreux (46% des cas). Les antihistaminiques étaient les plus utilisés à visée symptômatique dans 40% des cas.
DISCUSSION
Limite de l’étude
Comme toute étude, le caractère rétrospectif de ce travail milite en faveur de la perte de certaines données à savoir, l’absence de précision des différents sites lésionnels dans les dossiers des patients.
Données épidémiologiques
Au terme de notre étude, les toxidermies représentaient 2,85% des cas, soit 50 cas un total de 1750 PVVIH qui étaient inclus dans notre étude. Ce résultat concorde avec les données de la littérature selon lesquelles les toxidermies surviennent chez environ 2-3% des patients sous ARV [5,6].
Caractéristiques générales de la population
Nous avons constaté une prédominance féminine avec 76% (Tableau 4) et un sex ratio de 0,31. Ce résultat est comparable à celui de Caumes E et al. qui ont retrouvé un sexe ratio de 0,47. Il diffère de celui de Zannou D M et al. qui ont trouvé une prédominance masculin de 55,4% soit un sex ratio de 1,25. Ceci pourrait s’expliquer simplement par la vulnérabilité des femmes à l’infection à VIH en Afrique [5,6].
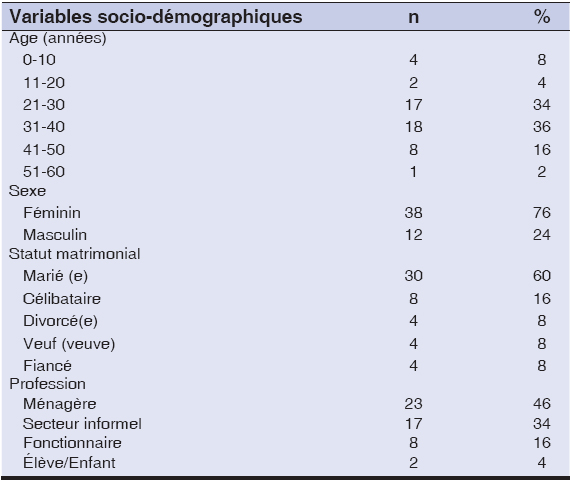 |
Tableau 4: Caractéristiques générales de la population. |
La tranche d’âge la plus représentée était celle de 31 à 40 ans soit 36% (Tableau 4) avec une moyenne de 30,8 ± 11,46 ans et des extrêmes de 4 et 60 ans. Ce résultat est comparable à celui de Zannou D M et a.l et de Koudema M qui ont trouvé respectivement une moyenne d’âge de 41 ans et 35,2 ans [5]. La majorité des patients inclus dans notre étude (84%) résidait à Bamako. Ceci s’explique par la stratégie thérapeutique de la politique nationale qui consiste à rapprocher le prestataire de santé du lieu de résidence des patients en vue de leur meilleure prise en charge [7]. Les mariés étaient majoritaires dans notre étude (Tableau 4) dans 60% des cas. Ce résultat est similaire à ceux d’autres auteurs qui ont rapporté le même constat [8–10]. Ceci pourrait s’expliquer par des pratiques socioculturelles notamment le lévirat, le sororat et le manque de diagnostic prénuptial du VIH.
DONNÉES CLINICOBIOLOGIQUES ET THÉRAPEUTIQUES
Liées au VIH
Sur les 1 750 dossiers des PVVIH, 1 474 avaient bénéficié du traitement ARV parmi les lesquels 48 avaient développé une toxidermie, 276 patients étaient non éligibles au traitement ARV dont 2 patients avaient présenté une toxidermie. Au total, 50 patients avaient ont donc développé une toxidermie soit 2,85% des cas. Le sérotype le plus représenté était le VIH1 (96%). Ce constat a été fait dans plusieurs autres études notamment celles de Onyemelukwe GC et al., de Zannou DM et al. et de Pitche P et al. [7–9]. La plupart de nos patients étaient au stade clinique III de l’OMS (Tableau 5) dans 48% des cas et ces patients étaient sous prophylaxie primaire au Cotrimoxazole avant la mise sous ARV. Notre étude a retrouvé un déficit immunitaire sévère chez 44% de nos patients avec un taux de CD4<200 cellules/mm3 (Tableau 3) à l’inclusion avec une moyenne de 228,10 cellules/mm3. Ce résultat est supérieur à celui de Kane et al. qui a trouvé une moyenne de 135,58 cellules/mm3 [10]. Ceci expliquerait le fait que le déficit immunitaire est un facteur de risque de toxidermie [11].
 |
Tableau 5: Répartition des PVVIH selon les données cliniques. |
Liées aux molécules incriminées
Dans notre étude nous avons recensé 28% de réactions au Cotrimoxazole (Tableau 1). Le même constat a été fait par Pitche et al. au Togo, qui montraient que 40% de ces réactions sont dues aux sulfamides chez les patients infectés par le VIH [9]. Les ARV ont été incriminés dans 62% des réactions et l’ARV associé au Cotrimoxazole dans 10% des cas de toxidermies de notre étude (Tableau 1). Ces résultats sont superposables à ceux déclarés par Kane et al. qui ont trouvé 43,2% des toxidermies liées aux ARV [10]. Les lésions liées au Cotrimoxazole ont été dominées par les prurits (16%) suivis d’urticaire (10%) et celles liées aux ARV ont été représentées par l’éxanthème maculo-papuleux (20%), résultats démontrés également par d’autres auteurs [10]. Dans notre étude, nous avons recensé un cas de syndrome de Lyell au cours de la coinfection VIH-tuberculose. Ce constat a été fait par Kouassi et al. qui ont obtenu trois cas de syndrome de Lyell dans une étude menée en Côte d’ivoire lors d’un traitement antituberculeux chez des patients séropositifs non traités [12]. Les ARV responsables ou fortement suspectés dans notre série de toxidermies sont la Névirapine (62%) et l’Efavirenz (10%). Nos résultats se rapprochent de ceux de Kane et al. qui a trouvé 52,6% pour Nevirapine [10], et de Caumes E et al. (34%) [7] pour l’Efavirenz. Ceci explique la recommandation dans le schéma thérapeutique en première ligne de ces ARV dans la politique nationale de prise en charge aux ARV. Ainsi les lésions liées à la Nevirapine étaient dominées par les exanthèmes (18%) suivis du syndrome de Lyell (12%). La responsabilité de la Névirapine dans le syndrome de Steven Johnson ou le syndrome de Lyell a déjà été notée par de nombreux auteurs [7,13]. Ceci s’expliquerait par la prolongation du temps de l’arrêt du médicament incriminé après l’apparition des lésions cutanées. Le délai écoulé entre l’introduction du médicament et l’apparition de la toxidermie varie en majorité entre 5jours et 30 jours (72%) avec un délai moyen de 23,5 ± 17,7 jours (Tableau 2). Un constat semblable a été fait par Kane et al. [10] avec un délai moyen de 16,9 jours mais aussi par d’autres auteurs [14] qui ont trouvé que 75% des patients sous ARV présentent des réactions cutanées dans un délai moyen de 10 jours [15]. La majorité des lésions dues au cotrimoxazole apparaissaient avant 15 jours (64,29%) et celle dues à la Nevirapine au-delà de 15 jours (70,83%).
Liées au traitement et à l’évolution
La plupart de nos patients (94%) ayant présenté une toxidermie ont été suivis aux USAC, seulement 6% d’entre eux ayant été référés en service de dermatologie pour une prise en charge. Le traitement était symptomatique et l’antihistaminique était utilisé chez tous nos malades (Tableau 6). Une modification de la combinaison ARV a été effectuée chez 72% de nos patients et l’arrêt du cotrimoxazole chez 28%. Nous avons constaté une évolution vers une guérison sans séquelles chez tous nos malades soit 100% des cas et aucun décès directement lié à la toxidermie n’avait été enregistré.
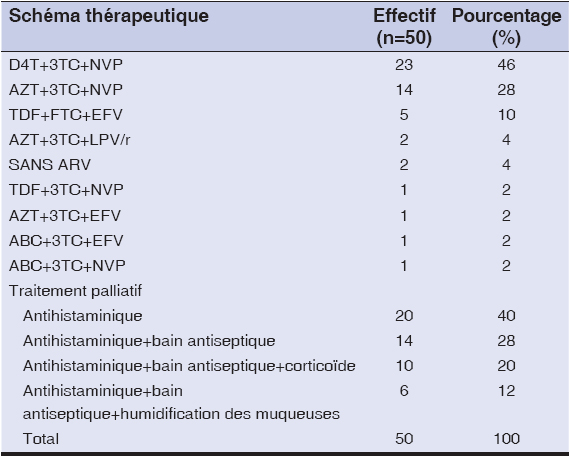 |
Tableau 6: Répartition des patients selon le schéma thérapeutique. |
CONCLUSION
Le présent travail relève que malgré leurs bénéfices thérapeutiques, les antirétroviraux sont pourvoyeurs des toxidermies sous toutes leurs formes cliniques, avec un pic élevé de des syndromes de Lyell et de Steven Johnson qui peuvent mettre en jeu le pronostic vital des personnes vivant avec le VIH. Une surveillance médicale rigoureuse s’avère donc indispensable en vue de prévenir leur survenue.
REMERCIEMENTS
Les auteurs remercient tous les PVVIH des deux unités retenues d’avoir accepté de participer à cette étude. Nous aimerions aussi saluer professeur Ousmane Faye pour son soutien aux jeunes chercheurs maliens. Nous remercions chaleureusement l’administration, pour toutes les facilités obtenues pour réaliser la présente étude.
RÉFÉRENCES
1. Drobacheff C, Laurent R, Antiretroviraux. In Dubertret L, Aractingi S, Bodemer C, Cribier B, Bachelez H, Choisidow O, Joli P. eds. Thérapeutique dermatologique;Flammarion Paris:2002;949-51.
2. Roujeau J, Wolkenstein P. Réactions cutanées aux médicaments. In Dermatologie et infections sexuellement transmissibles. 4edition Masson. Paris:2000;385-92.
3. Bulletin d’informations de pharmacovigilance. (Maroc). Toxidermies Médicamenteuses 2006;3(1):1-2.
4. Konaré HD, CisséI A, Oumar AA, Idrissa S, Maiga S, Dao S, et al. Toxidermie médicamenteuse en milieu hospitalier Bamako. Mali médical. 2012;27:57-61.
5. Zannou DM, Houngb F, Acapko J, Adé G, Gougounou A, Akondé A. Effets indésirables des thérapies antirétrovirales observés chez les patients infectés par le VIH, Cotonou, Bénin. Mali Méd. 2007;22:37-43.
6. Caumes E, Bossi P, Katlam C, Bricaire F. Toxidermies dues aux antirétroviraux chez les patients infectés par le VIH. Presse Med. 2003;33:1325-33.
7. Onyemelukwe GC, Musa BO. CD4+and CD8+lymphocytes and clinical features of HIV seropositive Nigerians on presentation. Afr J Med Med Sci. 2002;31:229-33.
8. Zannou DM, Kinde-Gazard D, Vigan J, Ade Sehonou G, Atadokpede F, Azondekon A, et al. Clinical and immunological profile of HIV infected patients in Cotonou, Benin. Med Mal Infect. 2004;34:225-8.
9. Pitche P, Mouzou T, Padonou C, Thangai- Wala K. Stevens Johnson syndrome and toxic epidermal necrolysis after intake of rifampicinisoniasid:report of 8 cases in HIV infected patients in Togo.Med Trop. 2005;65:359-62.
10. Kane A, Niang S, Kébé M, Ly F, Diallo M, Dieng MT, et al. Les effets secondaires dermatologiques des antirétroviraux (ARV) au Service de Dermatologie CHU Le Dantec Dakar. Mali Med Tome XXII 2007;23p.
11. Drobacheff-Thiebaut C, Gavignet B, Mercier M, Laurent R. Toxidermie à la névirapine: Étude des facteurs de risque chez 101 malades infectés par le VIH. Ann Dermatol Venererol. 2005;132:970-74.
12. Kouassi B, Horo K, Vilasco B. Syndrome de Lyell chez trois malades VIH (+) sous traitement antituberculeux. Rev Mal Resp. 2010;27:247-50.
13. Warren KJ, Boxwell DE, Kim NYet Drl BA. Nevirapine-associated Steven-Johnson syndrome. Lancet. 1998;351:567
14. Coopman SA, Johnson RA, Platt R, Stern RS. Cutaneous disease and drug réactions in HIV infection. N Engl J Med. 1993;328:1670-4.
15. Leclercq P, Roudière L, Viard JP. Complications graves des traitements antirétroviraux. Réanimation. 2004;13:238-48.
Notes
Source of Support: Nil,
Conflict of Interest: None declared.
Request permissions
If you wish to reuse any or all of this article please use the e-mail (brzezoo77@yahoo.com) to contact with publisher.
| Related Articles | Search Authors in |
|
 http://orcid.org/0000-0002-6657-4061 http://orcid.org/0000-0002-6657-4061 |



Comments are closed.