Cas fatal d’un syndrome de Lyell induit par ciprofloxacine chez un enfant
[Fatal case of toxic epidermal necrolysis induced by ciprofloxacin in a child]
Pharmacovigilance unit Pierre Fabre Laboratoire, 45 Place Abel Gance, 92100 Boulogne-Billancourt, France
Corresponding author: Thomas Schiestel, Pharm.D.
Submission: 14.12.2020; Acceptance: 10.01.2021
DOI: 10.7241/ourd.2021s1.6
Cite this article: Schiestel T. Cas fatal d’un syndrome de Lyell induit par ciprofl oxacine chez un enfant. [Fatal case of toxic epidermal necrolysis induced by ciprofl oxacin in a child]. Our Dermatol Online. 2021;12(Supp. 1):26-29.
Citation tools:
Copyright information
© Our Dermatology Online 2021. No commercial re-use. See rights and permissions. Published by Our Dermatology Online.
ABSTRACT
Bullous drug eruptions such as Toxic Epidermal Necrolysis (TEN) and Stevens-Johnson syndrome (SJS) are rare but known adverse reactions of fluoroquinolones. Although uncommon, TEN can be life-threatening for the patient, especially in the context of delayed treatment and in fragile patients such as the pediatric population. In the present case, TEN occurred in a 13-year-old girl with no medical history following initiation of ciprofloxacin treatment for an inguinal cyst. We hope that the case report will make interrogate the practices concerning the use of antibiotics, in particular fluoroquinolones in the context of an use not prescribed by the Marketing Authorization of the drug in children.
Key words: Toxic Epidermal Necrolysis; ciprofloxacin; quinolone; child; pediatric; death
RÉSUMÉ
Les toxidermies bulleuses telles que la Nécrolyse Epidermique Toxique (NET) et le syndrome de Stevens-Johnson (SSJ) sont des reactions secondaires rares mais connues des fluoroquinolones. Bien que peu commune, la NET peut engager le prognostic vital du patient, notamment dans la cadre d’un retard de prise en charge et lorsqu’il s’agit de patients fragiles comme la population pédiatrique. Dans le cas que nous présentons, une NET est survenue chez une jeune fille de 13 ans sans antécédents dans les suites de l’instauration d’un traitement par ciprofloxacine dans le cadre d’un kyste inguinal. Nous souhaitons que ce cas rapporté permettra de remettre en cause les pratiques concernant l’usage d’antibiotiques, notamment les fluoroquinolones dans un usage non prescrit par l’Autorisation de Mise sur le Marché (AMM) du medicament chez l’enfant.
Mots clés: Nécrolyse épidermique toxique; ciprofloxacine; quinolone; enfant; pédiatrique; décès
INTRODUCTION
La Nécrolyse Epidermique Toxique (NET) ou syndrome de Lyell fait partie avec le syndrome de Stevens-Johnson (SSJ) des toxidermies bulleuses sévères [1]. La différence majeure entre ces deux pathologies concerne l’extension des lésions de l’épidermolyse : moins de 10% pour le SJS, plus de 30% pour le NET et entre 10 et 30% en cas de « chevauchement » [2]. Dans les deux affections, les atteintes d’organe sont très fréquentes : muqueuses, système digestif, yeux, reins, poumons [3]. Si des lacunes subsistent quant aux causes du NET, une réaction d’hypersensibilité de type IV impliquant plusieurs classes de médicaments reste l’hypothèse la plus partagée. Les médicaments les plus associés aux NET sont les antibiotiques (sulfonamides, pénicilline, céphalosporine, quinolones), la carbamazépine, l’allopurinol et les anti-inflammatoires non-stéroïdiens entre autres [4]. Une étude de cohorte américaine avait rapporté une fréquence de NET de 0,5/100 000 enfants hospitalisés par an [2]. Les enfants représenteraient ainsi 20% des cas atteints de NET [5]. Ici, nous rapportons un cas de NET d’issue fatale chez une jeune fille de 13 ans sans antécédents à plus d’un mois d’un traitement par ciprofloxacine pour un kyste inguinal. Avec ce cas dramatique, nous souhaitons insister sur le contexte très particulier de survenue de ce NET, à savoir une prescription hors-AMM, en particulier chez un enfant.
CASE REPORT
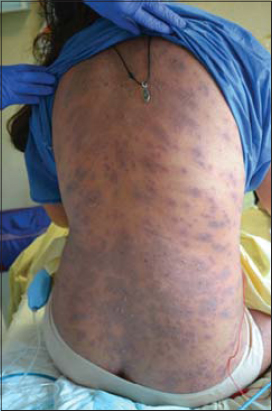
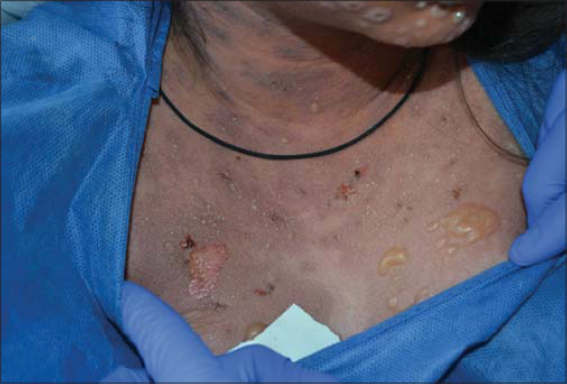
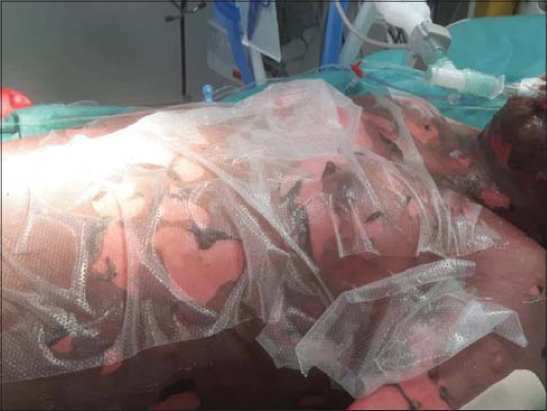
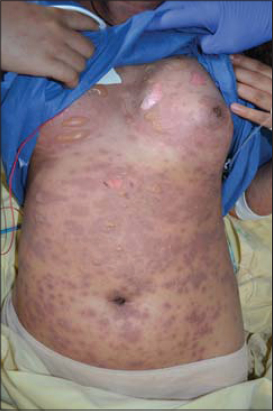
La patiente de 13 ans n’a pas d’antécédents particuliers ni d’allergie. Elle ne prend aucun traitement au long cours. Le 24 mars 2019, elle débute un traitement par ciprofloxacine 2 comprimés par jour (dosage non précisé) pour une durée de 10 jours pour un kyste inguinal volumineux droit. – Le traitement prend fin le 2 avril 2019. Le 04 avril 2019 au matin : Apparition des lesions cutanées de manière progressive (visage, thorax puis généralisée) ; Evolution des lesions vers des vésicules/bulles du visage et du tronc (Fig. 1). Le 6 avril au matin, la patiente est amenée aux urgences. L’examen clinique montre une conjonctivite vers 22h00 et une éruption cutanée vésiculeuse febrile (Fig. 2). Les signaux vitaux sont alors les suivants : temperature : 40,4°C, saturation : 100% en air ambiant, pression artérielle : 117/53 mmHg, fréquence cardiaque : 106/min, fréquence respiratoire : 21/min. L’exament biologique est normal excepté une proteine C-reactive à 99mg/L. Il n’y a pas d’atteinte d’organe ni de documentation virologique et bactériologique. Le diagnostic est posé : dermatose bulleuse avec lésions bulleuses des lèvres avec exsudat jaunâtre, lésions vésiculeuses et bulleuses du thorax avec contenu clair, lésions papuleuses des membres, lésions vésiculeuses des paumes et des plantes, plaque violacée dans l’intérieur des cuisses. érythème conjonctival et prurit oculaire. Les zones décollées représentent moins de 10% de la surface corporelle. Devant le tableau clinique, il est décidé une instauration d’une antibiothérapie par amoxicilline/acide clavullanique, clindamycine et azithromycine ainsi que des soins locaux et un traitement antalgique. Le 8 avril 2019, la patiente est transferée en reanimation. Elle présente alors une peau purpura surmontée d’une bulle sur fond érythrodermique, une desquamation à 6% et une surface décollable à peu près à 30% (Fig. 3). A partir du 10 avril, la patiente aura des difficultés respiratoires avec épisodes d’hypotensions artérielles et apparition d’une dysfonction myocardique (fraction d’ejection : 40%), un choc septique à Entérocoque Faecalis. Le 17 avril, le décollement va atteindre 90% malgré les soins de supports (Fig. 4). Le 30 avril 2019 survient une aggravation de l’extension du décollement jusqu’à 100% avec de multiples complications : détresse respiratoire aiguë, état de choc, ulcération oesophagienne sanglante, insuffisance rénale aiguë, atteinte hépatique cytolytique et cholestatique dans un contexte de défaillance multiviscérale, choc septique. Le 30 avril 2019, la patiente est en état de choc distributif réfractaire avec défaillance multi-viscérale malgré l’optimisation des thérapeutiques médicales usuelles. La patiente décède le 1er mai 2019.
CONCLUSION
La mortalité associée aux toxidermies bulleuses est conséquente : entre 30 et 35% pour la NET, 5% pour le SSJ [6]. Toute population confondue, Les NET et les SSJ seraient provoqués dans 72 à 90% des cas par un médicament [2]. Plus précisément, la littérature mentionne plusieurs cas de toxidermie bulleuse (NET ou SSJ) sous fluoroquinolones (ciprofloxacine, ofloxacine, levofloxacine, norfloxacine, moxifloxacine) chez des patients adultes [7–11]. Cependant, dans la population pédiatrique, nous n’avons pas trouvé de cas de NET ou SSJ sous fluoroquinolone. Dans une étude rétrospective, 12 cas de dermatoses bulleuses pédiatriques ont été analysés [12]. 4 cas ont été associés à une infection et 8 à l’utilisation d’un médicament ; les complications, pour sévères qu’elles étaient n’ont pas eu d’issue fatale dans aucun des cas. Les fluoroquinolones sont indiqués dans les infections respiratoires et les infections urinaires entre autres. Dans le cas rapporté, l’utilisation de ciprofloxacine dans le cadre d’un kyste était hors-AMM ; il est urgent que les prescripteurs soient éduqués sur les risques associés à l’utilisation des fluoroquinolones, en particulier dans la population pédiatrique.
Remerciements
Nous souhaitons remercier tout particulièrement le service de Pharmacologie Pédiatrique et Pharmacogénétique, Hôpital Robert Debré, Bd Sérurier, 75019 Paris, France, pour nous avoir adressé ce cas.
Consent
The examination of the patient was conducted according to the principles of the Declaration of Helsinki.
The authors certify that they have obtained all appropriate patient consent forms, in which the patients gave their consent for images and other clinical information to be included in the journal. The patients understand that their names and initials will not be published and due effort will be made to conceal their identity, but that anonymity cannot be guaranteed.
RÉFÉRENCES
1. Tounkara TM, BaldéH, Soumah MM, Bangoura M, DianéBF, Keita M et al. Severe cutaneous drug reactions in Guinean children:a monocentric retrospective study of 35 cases. Our Dermatol Online. 2018;9:118-22.
2. Ramien M, Goldman J L. Pediatric SJS-TEN:Where are we now?F1000Res. 2020;9:F1000 Faculty Rev-982.
3. Liotti L, Caimmi S, Bottau P, Bernardini R, Cardinale F, Saretta F, et al. Clinical features, outcomes and treatment in children with drug induced Stevens-Johnson syndrome and toxic epidermal necrolysis. Acta Biomed. 2019;90(3-S):52-60.
4. Harr T, French L. Toxic epidermal necrolysis and Stevens-Johnson syndrome. Orphanet J Rare Dis. 2010;5:39.
5. Sotelo-Cruz N. Stevens-Johnson syndrome and toxic epidermal necrolysis in children. Author reply. Gac Med Mex. 2013;149:113-4.
6. Lezcano L, Di Martino Ortiz B, Rodríguez Masi M, Knopfelmacher O, Bolla de Lezcano L. [Toxical epidermal necrolysis. Report of two cases. Severe skin rash caused by common drugs]. Our Dermatol Online. 2013;4:517-21.
7. Livasy C, Kaplan A. Ciprofloxacin-induced toxic epidermal necrolysis:a case report. Dermatology. 1997;195:173-5.
8. Vaghela J, Nimbark V, Chavda B, Mehta H, Purohit B. A Rare Case Report of Toxic Epidermal Necrolysis Due to Ofloxacin. Curr Drug Saf. 2018;13:137-40.
9. Rusen U, Arzu Y, Betul C, Tangul B, Ata Y. Levofloxacin Induced Toxic Epidermal Necrolysis:Successful Therapy with Omalizumab (Anti-IgE) and Pulse Prednisolone. Am J Case Rep. 2016;17:666-71.
10. Maciejewska J, Jankowski M, Zegarska B, Czajkowski R. Stevens-Johnson syndrome/toxic epidermal necrolysis presumably induced by norfloxacin. Postep Derm Alergol. 2014;XXXI:194–6.
11. Howard-Thompson A, Cartmell B, Suda K. Toxic epidermal necrolysis reaction associated with the use of moxifloxacin. Int J Antimicrob Agents. 2014;44:178-9.
12. Sato S, Kanbe T, Tamaki Z, Furuichi M, Uejima Y, Suganuma E et al. Clinical features of Stevens-Johnson syndrome and toxic epidermal necrolysis. Pediatr Int. 2018;60:697-702.
Notes
Source of Support: Nil,
Conflict of Interest: None declared.
Request permissions
If you wish to reuse any or all of this article please use the e-mail (brzezoo77@yahoo.com) to contact with publisher.
| Related Articles | Search Authors in |
|
|




Comments are closed.